
Термин «коррозия» походит от латинского слова «corrodere», что означает «разъедать» что либо.
Коррозия - это самопроизвольное разрушение металлов под воздействием химического или физико-химического влияния окружающей среды. В широком понимании, коррозии подвергаются не только металлы, но и любые материалы, будь то бетон, пластмасса, резина или керамика.
Причиной возникновения и протекания процессов коррозии является термодинамическая неустойчивость материалов к определенным компонентам, находящихся в окружающей их среде. Результатом коррозии являются продукты коррозии (например, ржавчина), испорченное оборудование, разрушение конструкций.
Ежегодно коррозия наносит огромнейший ущерб народному хозяйству каждой страны. В промышленно развитых странах убытки от коррозии за год составляют в среднем около 3 - 5% от внутреннего валового продукта. А потери металла достигают 20%. Ущерб от коррозии складывается не только от стоимости материалов, но и от затрат на изготовление пришедших в негодность конструкций, оборудования и различных изделий.
Коррозия наносит как прямые, так и косвенные убытки.
К косвенным относятся убытки, связанные с отказом оборудования, пришедшего в негодность из-за коррозионных процессов, его простоя, замены или ремонта, порчей продукции других производств в следствии загрязнения ее продуктами коррозии, высокими допусками на коррозию, стоимость дополнительно потраченной электроэнергии, воды, материалов и др.
К прямым - стоимость испорченных коррозией трубопроводов, оборудования, машин и др.
Коррозию по механизму протекания принято разделять на химическую и электрохимическую. Более распространенный - второй вид.
Наука о коррозии и защите металлов изучает особенности и механизмы протекания коррозионных процессов в различных средах. Задачей науки о коррозии является не только изучение, но и разработка методов защиты различных материалов от коррозии.
Наука о коррозии подразумевает не только знание всех закономерностей протекания процессов коррозии. Нужно еще и хорошо знать свойства металлов, различных материалов. При изучении коррозии металлов и методов защиты от нее, научной базой является физическая химия и металловедение.
Важно знать, что коррозия – это многостадийный сложный процесс, который необходимо изучать целостно. Только изучив саму суть коррозионного процесса, можно приступать к изучению и разработке методов защиты.
В основе коррозийных процессов лежат окислительно-восстановительные реакции металлов с окружающей средой, сопровождающиеся переходом металлов в более термодинамически устойчивое состояние.
Рассмотрим коррозию железа как электрохимический процесс. Ржавление железа есть не что иное, как анодная реакция
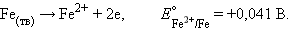
Катодная реакция – восстановление атмосферного кислорода:
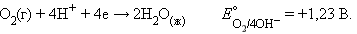
Водородные ионы поставляет вода. Если бы в воде не было растворенного кислорода, то коррозия была бы невозможна. Следовательно, железо корродирует в слое воды, насыщенном кислородом. Таким образом, начальную стадию коррозии железа можно передать реакцией
| 2Fe + O2 + 4H+ → 2FeO + 2H2O. |
На скорость коррозии существенное влияние оказывает концентрация ионов H+. Повышение pH приводит к замедлению коррозии, поскольку восстановление O2 из H2O замедляется. При pH = 9–10 коррозия железа практически прекращается. Известно, что в водной среде ионы Fe2+ в присутствии кислорода окисляются до Fe3+. Вторая стадия коррозии соответствует реакции образования гидратированного оксида железа (ржавчины) Fe2O3∙nH2O (рис. 7.4):
| 4Fe2+ + O2 + 4H2O + xH2O = 2Fe2O3∙xH2O + 8H+. |
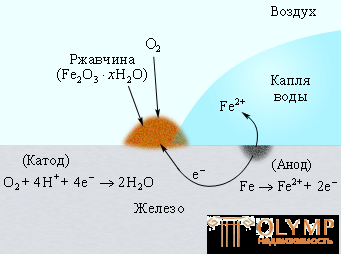 Рисунок 7.4
Рисунок 7.4
Коррозия железа кислородом воздуха, растворенным в воде
Для защиты железа от коррозии используются всевозможные покрытия: краска, слой металла (олова, цинка). При этом краска и олово предохраняют от коррозии до тех пор, пока защитный слой цел. Появление в нем трещин и царапин способствует проникновению влаги и воздуха к поверхности железа, и процесс коррозии возобновляется, причем в случае оловянного покрытия он даже ускоряется, поскольку олово служит катодом в электрохимическом процессе (рис. 7.5).
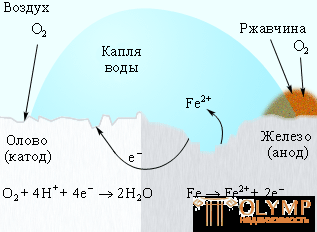 Рисунок 7.5
Рисунок 7.5
Коррозия «белой жести»
Оцинкованное железо ведет себя иначе. Поскольку цинк выполняет роль анода, то его защитная функция сохраняется и при нарушении цинкового покрытия (рис. 7.6).
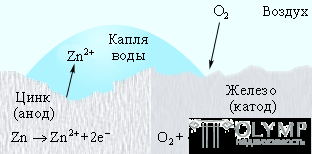 Рисунок 7.6
Рисунок 7.6
Катодная защита в оцинкованном железе
Катодная защита широко используется для уменьшения коррозии подземных и подводных трубопроводов и стальных опор высоковольтных передач, нефтяных платформ и причалов.
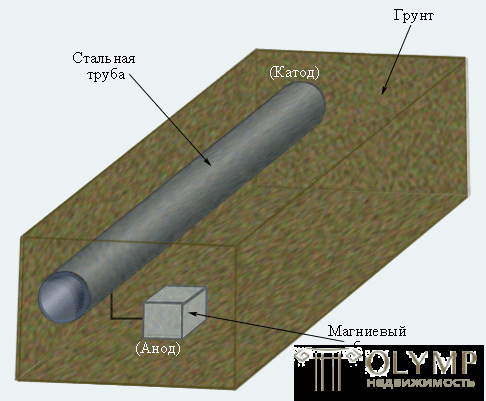 Рисунок 7.7
Рисунок 7.7
Катодная защита подземного трубопровода
Химическая коррозия - это вид коррозионного разрушения металла, связанный с взаимодействием металла и коррозионной среды, при котором одновременно окисляется металл и происходит восстановление коррозионной среды. Химическаякоррозия не связана с образованием, а также воздействием электрического тока.
Движущей силой (первопричиной) химической коррозии является термодинамическая неустойчивость металлов. Они могут самопроизвольно переходить в более устойчивое состояние в результате процесса:
Металл + Окислительный компонент среды = Продукт реакции
При этом термодинамический потенциал системы уменьшается.
По знаку изменения термодинамического потенциала можно определить возможность самопроизвольного протекания химической коррозии. Критерием обычно служит изобарно-изотермический потенциал G. При самопроизвольном протекании химического процесса наблюдается убыль изобарно-изотермического потенциала. Поэтому, если:
Δ GТ < 0, то процесс химической коррозии возможен;
Δ GТ > 0, то процесс химической коррозии невозможен;
Δ GТ = 0, то система находится в равновесии.
К химической коррозии относятся:
- газовая коррозия - коррозионное разрушение под воздействием газов при высоких температурах;
- коррозия в жидкостях-неэлектролитах.
Газовая коррозия - наиболее распространенный вид химической коррозии. При высоких температурах поверхность металла под воздействием газов разрушается. Это явление наблюдается в основном в металлургии (оборудование для горячей прокатки, ковки, штамповки, детали двигателей внутреннего сгорания и др.)
Самый распространенный случай химической коррозии – взаимодействие металла с кислородом. Процесс протекает по реакции:
Ме + 1/2О2 - МеО
Направление этой реакции (окисления) определяется парциальным давлением кислорода в смеси газов (pО2) и давлением диссоциации паров оксида при определенной температуре (рМеО).
Эта химическая реакция может протекать тремя путями:
1) pО2 = рМеО, реакция равновесная;
2) pО2 > рМеО, реакция сдвинута в сторону образования оксида;
3) pО2 < рМеО, оксид диссоциирует на чистый металл и оксид, реакция протекает в обратном направлении.
Зная парциальное давление кислорода газовой смеси и давление диссоциации оксида можно определить интервал температур, при которых термодинамически возможно протекание данной реакции.
Скорость протекания газовой коррозии определяется несколькими факторами: температуры окружающей среды, природы металла или состава сплава, характера газовой среды, времени контакта с газовой средой, от свойств продуктов коррозии.
Процесс химической коррозии во многом зависит от характера и свойств образовавшейся на поверхности оксидной пленки.
Процесс появления на поверхности оксидной пленки можно условно разделить на две стадии:
- на поверхности металла, которая непосредственно контактирует с атмосферой, адсорбируются молекулы кислорода;
- металл взаимодействует с газом с образованием химического соединения.
На первой стадии между поверхностными атомами и кислородом возникает ионная связь: атом кислорода забирает у металла два электрона. При этом возникает очень сильная связь, намного сильнее, чем связь кислорода с металлом в окисле. Возможно это явление наблюдается из-за действия на кислород поля, создаваемого атомами металла. После полного насыщения поверхности окислителем, что происходит почти мгновенно, при низких температурах за счет ванн-дер-вальсовых сил может наблюдаться и физическая адсорбция молекул окислителя.
В результате образуется очень тонкая мономолекулярная защитная пленка, которая со временем утолщается, затрудняя подход кислорода.
На второй стадии, из-за химического взаимодействия, окислительный компонент среды отнимает у металла валентные электроны и с ним же реагирует, образуя продукт коррозии.
Если образовавшаяся оксидная пленка будет обладать хорошими защитными свойствами - она будет тормозить дальнейшее развитие процесса химической коррозии. Кроме того, оксидная пленка очень сильно влияет на жаростойкость металла.
Существует три вида пленок, которые могут образоваться:
- тонкие (невидимые невооруженным глазом);
- средние (дают цвета побежалости);
- толстые (хорошо видны).
Чтобы оксидная пленка была защитной, она должна отвечать некоторым требованиям: не иметь пор, быть сплошной, хорошо сцепляться с поверхностью, быть химически инертной по отношении к окружающей ее среде, иметь высокую твердость, быть износостойкой.
Если пленка рыхлая и пористая, кроме того имеет еще плохое сцепление с поверхностью - она не будет обладать защитными свойствами.
Существует условие сплошности, которое формулируется так: молекулярный объем оксидной пленки должен быть больше атомного объема металла.
Сплошность - способность окисла покрывать сплошным слоем всю поверхность металла.
Если это условие соблюдается, то пленка сплошная и, соответственно, защитная.
Но есть металлы, для которых условие сплошности не является показателем. К ним относятся все щелочные, щелочно-земельные (кроме бериллия), даже магний, который важен в техническом плане.
Для определения толщины образовавшейся на поверхности оксидной пленки, изучения ее защитных свойств применяют множество методов. Защитную способность пленки могут определять во время ее формирования, по скорости окисления металла и характеру изменения скорости во времени. Если окисел уже сформировался, целесообразно исследовать толщину и защитные его свойства, нанося на поверхность какой-нибудь подходящий для этого случая реагент (например раствор Cu(NO3)2, который применяется для железа). По времени проникновения реагента к поверхности можно определить толщину пленки.
Даже уже образовавшаяся сплошная пленка не прекращает своего взаимодействия с металлом и окислительной средой.
Влияние внешних и внутренних факторов на скорость протекания химической коррозии.
На скорость химической коррозии очень сильное влияние оказывает температура. При ее повышении процессы окисления идут намного быстрее. При этом уменьшение термодинамической возможности протекания реакции не имеет никакого значения.
Особенно сильно влияет переменный нагрев и охлаждение. В защитной пленке вследствие появления термических напряжений образуются трещины. Сквозь трещины окислительный компонент среды имеет непосредственный доступ к поверхности. Формируется новая оксидная пленка, а старая - постепенно отслаивается.
Большую роль в процессе коррозии играет состав газовой среды. Но это индивидуально для каждого металла и изменяется с колебаниям температур. Например, медь очень быстро корродирует в атмосфере кислорода, но устойчива в среде, содержащей SO2. Никель же наоборот, интенсивно корродирует при контакте с атмосферой SO2, но устойчив в средах O2, CO2и H2O. Хром относительно устойчив во всех четырех средах.
Если давление диссоциации окисла выше давления окисляющего компонента - окисление металла прекращается, он становится термодинамически устойчивым.
Скорость окисления зависит от состава сплава. Возьмем, к примеру, железо. Добавки серы, марганца, фосфора и никеля не влияют на его окисление. Кремний, хром, алюминий - замедляют процесс. А бериллий, кобальт, титан и медь очень сильно тормозят окисление. При высоких температурах интенсифицировать процесс могут вольфрам, молибден, а также ванадий. Это объясняется летучестью или легкоплавкостью их окислов.
Наблюдая за скоростью окисления железа при различных температурах, отметим что с увеличением температуры самое медленное окисление наблюдается при аустенитной структуре. Она является наиболее жаростойкой, по сравнению с другими.
На скорость протекания химической коррозии влияет и характер обработки поверхности. Если поверхность гладкая, то она окисляется немного медленнее, чем бугристая поверхность с дефектами.
Жидкости-неэлектролиты - это жидкие среды, которые не являются проводниками электричества. К ним относятся: органические (бензол, фенол, хлороформ, спирты, керосин, нефть, бензин); неорганического происхождения (жидкий бром, расплавленная сера и т.д.). Чистые неэлектролиты не реагируют с металлами, но с добавлением даже незначительного количества примесей процесс взаимодействия резко ускоряется. Например, если нефть будет содержать серу или серосодержащие соединения (сероводород, меркаптаны) процесс химической коррозии ускоряется. Если вдобавок увеличится температура, в жидкости окажется растворенный кислород - химическая коррозия усилится.
Присутствие в жидкостях-неэлектролитах влаги обеспечивает интенсивное протекание коррозии уже по электрохимическому механизму.
Химическая коррозия в жидкостях-неэлектролитах подразделяется на несколько стадий:
- подход окислителя к поверхности металла;
- хемосорбция реагента на поверхности;
- реакция окислителя с металлом (образование оксидной пленки);
- десорбция оксидов с металлом (может отсутствовать);
- диффузия оксидов в неэлектролит (может отсутствовать).
Для защиты конструкций от химической коррозии в жидкостях-неэлектролитах на ее поверхность наносят покрытия, устойчивые в данной среде.
В данном разделе описаны способы защиты строительных материалов от коррозии в условиях агрессивных сред.
Всякая конструкция, кроме чисто силовых воздействий, вызывающих объемное напряженное состояние, подвергается физико-химическим воздействиям окружающей среды.
Среда может, быть в газообразном, жидком или твердом виде, а чаще всего — многофазной. Так, например, на фундаменты может действовать прилегающий к ним грунт (преимущественно насыщающие его грунтовые воды); на стены и покрытия действует наружная и внутренняя атмосфера разной влажности и загрязненности.
Отдельные агенты среды характеризуются большей или меньшей агрессивностью по отношению к различным материалам конструкций, т. е. способностью за определенный срок вызывать полное или частичное их разрушение.
Строго говоря, всякая среда воздействует на конструкцию. Эти воздействия могут быть либо агрессивными (чаще всего), либо благоприятными, способствующими стабилизации и даже упрочнению материала.
Основными задачами являлись: оценка агрессивности разных сред, описание действия среды на материалы и конструкции, составление рекомендаций по выбору материалов, стойких к данным средам; главное внимание при этом уделено воздействиям химических агентов и защите от них материалов и конструкций.
Задача проектировщика, назначающего тот или иной материал для применения в конструкциях с наличием агрессивных сред, ответственна и достаточно сложна. Применение относительно экономичных, но часто недостаточно стойких материалов приводит к быстрому их разрушению и высоким затратам на ремонтно-восстановительные работы; использование же высокостойких, но обычно более дорогих материалов увеличивает затраты на. возведение сооружений.
Идеальным решением, по-видимому, было бы проектирование равностойких элементов сооружений, которые разрушались бы одновременна и только после длительного (заданного) срока службы, соответствующего моральному износу оборудования. Однако практически это не всегда возможно. Поэтому в процессе эксплуатации зданий и сооружений приходится, к сожалению, довольно часто заменять быстроразрушающиеся элементы или отдельные конструкции — обычно полы, реже фундаменты, стены, покрытия и другие. В таких случаях при проектировании капитального ремонта на отдельных предприятиях желательно предусматривать возможность посекционной замены конструкций: это ускорит ремонтно-строительные работы и позволит выполнять их в условиях действующего предприятия без нарушения общего хода технологического процесса.
Среда воздействует преимущественно на поверхностные слои конструкций, постепенно проникая в глубину, особенно если материал недостаточно плотный. Поэтому очень часто защита конструкций от агрессивных воздействий среды сводится к уплотнению материала в поверхностном слое или нанесению достаточно плотных и стойких к данной среде защитных покрытий — облицовок, штукатурок, оклеечной изоляции или даже окраски. Естественно, что в период эксплуатации зданий и сооружений эти защитные покрытия должны периодически и своевременно обновляться.
Учитывая данные обстоятельства, механизм коррозионных процессов рассмотрен на сайте применительно к отдельным материалам, из которых изготовляются конструкции,— металлу, бетону, древесине, — или к материалам, которые наносятся на конструкции в качестве защитных покрытий,— краскам, пластикам, мастикам и растворам.
Значительное место занимает описание приемов повышения плотности и стойкости обычного цементного бетона, что вполне закономерно: он используется на строительстве; цементные бетоны высокой плотности являются достаточно экономичными и стойкими конструктивными и защитными (для металла) материалами во многих средах, за исключением сильнокислых вод.
Для повышения стойкости материалов и конструкций, работающих в кислых средах, рекомендуются специальные мастики, растворы и бетоны на жидком стекле, серном цементе и битуме.
При наличии переменных (кислото-щелочных) воздействий либо при воздействии высококонцентрированных или подогретых химических растворов необходимо применение более стойких материалов — на основе пластмасс и пластбетонов.
Для первичной защиты строительных конструкций от коррозии используют коррозионно-стойкие для данной среды покрытия. При необходимости предусматривают вторичную защиту поверхности конструкции:
• лакокрасочными покрытиями;
• оклеечной изоляцией из листовых и пленочных материалов;
• облицовкой, футеровкой, применением изделий из керамики, шлакоситалла, стекла, каменного литья, природного камня;
• штукатурными покрытиями на основе цемента, полимерных вяжущих, жидкого стекла, битума;
• уплотняющей пропиткой химически стойкими материалами.
По степени воздействия на строительные конструкции среды разделяются на неагрессивные, слабоагрессивные, среднеагрессивные и сильноагрессивные. По физическому состоянию среды подразделяют на газообразные, твердые и жидкие, а по характеру воздействия на материал конструкции — на химически и биологически активные.
Для бетонных и железобетонных конструкций, предназначенных для эксплуатации в агрессивной среде, при их проектировании коррозионную стойкость обеспечивают применением коррозионно-стойких составляющих, добавок, повышающих коррозионную стойкость самого бетона и его защитную способность для стальной арматуры. В изготовляемых конструкциях должны быть снижены проницаемость бетона, трещиностойкость, ширина расчетного раскрытия трещин и толщина защитного слоя бетона.
В случае недостаточной эффективности антикоррозийной защиты при изготовлении конструкций следует дополнительно предусмотреть их защиту:
• лакокрасочными покрытиями (аэрозолями) — при действии газообразных и твердых сред;
• лакокрасочными мастичными многослойными покрытиями — при действии жидких сред, при непосредственном контакте покрытия с твердой агрессивной средой;
• оклеечными покрытиями — при действии жидких сред, при расположении конструкции в грунте, в качестве непроницаемого слоя в облицовочных покрытиях;
• облицовочными покрытиями, в том числе из полимербетонов — при действии жидких сред, при расположении конструкции в грунте, в качестве защиты от механических повреждений оклеечного покрытия;
• уплотняющей пропиткой химически стойкими материалами — при действии жидких сред и грунта;
• гидрофобизацией — при периодическом увлажнении водой или атмосферными осадками, образовании конденсата, в качестве грунтового слоя под лакокрасочное покрытие.
Меры защиты железобетонных конструкций от коррозии назначаются в проекте производства работ с учетом вида и особенностей защищаемых конструкций, технологии их изготовления, возведения и условий эксплуатации.
Для бетонных и железобетонных конструкций зданий и сооружений с агрессивными средами необходимо предусматривать применение только следующих цементов: портландцемента, шлакопортландцемента, сульфатостойкого, глиноземистого и напрягающего цементов. Не допускается введение хлористых солей в состав бетона для железобетонных конструкций, а также в растворы для инъецирования каналов, замоноличивания швов и стыков конструкций.
Толщину защитного слоя бетона для плоскостных конструкций допускается применять равной 15 мм для слабоагрессивной и среднеагрессивной сред и равной 20 мм — для сильноагрессивной среды. Для аналогичных монолитных конструкций необходимая толщина защитного слоя повышается на 5 мм.
Закладные детали и соединительные элементы в стыках конструкций, подверженные воздействию жидкой среды, должны быть защищены металлическими или комбинированными покрытиями. На поверхностные закладные детали необходимо в обязательном порядке наносить лакокрасочные покрытия.
Толщина металлизационных покрытий и металлизационного слоя в комбинированных покрытиях должна быть для цинковых и алюминиевых покрытий не менее 120 мкм. Толщина цинковых покрытий, получаемых горячим цинкованием, должна быть не менее 50 мкм, а гальваническим способом — не менее 30 мкм.
Для защиты деревянных конструкций от коррозии, вызываемой воздействием биологических агентов, применяют антисептирование, консервирование, покрытие лакокрасочными материалами или поверхностную пропитку составами комплексного действия. Если конструкция окажется в химически агрессивной среде, то для защитного покрытия лакокрасочные материалы или пропитку составами комплексного действия.
В зависимости от степени агрессивного воздействия деревянные конструкции защищают водорастворимыми и трудновымываемыми антисептиками или путем обработки поверхности антисептическими пастами. Защитные покрытия выполняют из влагостойких лакокрасочных материалов или влагобиозащитных пропиточных составов.
Для защитных покрытий древесины применимы лаки и эмали пентафталевые, перхлорвиниловые, эпоксидные, эпоксидно-фенольные и др. Антисептирование рекомендуется выполнять фтористым натрием, аммонием кремнефтористым, специально разработанными для антисептирования препаратами. При консервировании древесины лучшими препаратами признаны масло каменноугольное, антраценовое и сланцевое.
Для химической защиты деревянных конструкций разработаны химически стойкие, влагостойкие лакокрасочные материалы и химически стойкие влагостойкие пропиточные составы.
Каменные и асбестоцементные конструкции. Агрессивное воздействие на конструкции из этих материалов может быть газообразным, жидким. При засоленных грунтах и жидких агрессивных средах не разрешается применение конструкций из силикатного кирпича, а также строительных растворов с использованием глины и золы. При периодическом увлажнении агрессивной средой и замораживании кладки марку кирпича по морозостойкости следует принимать не ниже F50. При сильноагрессивной степени воздействия кислых сред следует применять для кладки кислотостойкие растворы на основе жидкого стекла или полимерных связующих.
Поверхности каменных и армокаменных конструкций от коррозии необходимо дополнительно защищать: по штукатурке — лакокрасочным покрытием, непосредственно по каменной кладке — многослойными мастичными материалами.
Асбестоцементные стеновые панели не должны соприкасаться с грунтом. Эти конструкции необходимо располагать на цоколе, имеющем гидроизоляционную прокладку, предохраняющую панели от капиллярного подсоса агрессивных грунтовых вод. Поверхность асбестоцементных конструкций следует защищать от агрессивного воздействия сред лакокрасочными покрытиями, такими же как и для бетонных конструкций.
Металлические конструкции должны покрываться антикоррозионными покрытиями при агрессивном воздействии сред — атмосферы воздуха, жидких органических и неорганических сред, грунтов.
Несущие конструкции из алюминия должны быть защищены от коррозии путем электрохимического анодирования (толщина слоя > 15 мкм). При эксплуатации конструкций в воде они должны быть дополнительно окрашены водостойкими лакокрасочными материалами.
Примыкание конструкций из алюминия к конструкциям из кирпича или бетона допускается только после полного твердения раствора или бетона независимо от степени агрессивного воздействия среды. Участки примыкания должны быть защищены лакокрасочными покрытиями. Обетонирование конструкций из алюминия не допускается. Примыкание окрашенных конструкций из алюминия к деревянным допускается при условии пропитки последних креозотом.
Для защиты стальных и алюминиевых конструкций от коррозии применяют лакокрасочные материалы (грунтовки, краски, эмали, лаки), разбитые в зависимости от степени агрессивного воздействия среды на четыре группы:
I — пентафталевые, глифталевые, эпоксиэфирные, алкидно-стирольные, масляные, масляно-битумные, алкидно-уретановые, нитроцеллюлозные;
II — фенолформальдегидные, хлоркаучуковые, перхлорвиниловые, поливинилбутиральные, полиакриловые, акрил силиконовые, полиэфирсиликоновые, сланцевиниловые;
III— эпоксидные, кремнийорганические, перхлорвиниловые, сланцевиниловые, полистирольные, полиуретановые, фенолформальдегидные;
IV— перхлорвиниловые и эпоксидные.
Горячее цинкование и алюминирование методом погружения в расплав необходимо предусматривать для защиты от коррозии стальных конструкций с болтовыми соединениями, а также болтов, гаек и шайб. Газотермическое напыление цинка и алюминия необходимо предусматривать для защиты стальных конструкций со сварными, болтовыми и заклепочными соединениями. Электрохимическая защита является обязательной для стальных конструкций, погружаемых в грунт или в неорганические жидкие среды, внутренних поверхностей днищ резервуаров для нефти и нефтепродуктов.
Химическое оксидирование с последующим окрашиванием или электрохимическое анодирование поверхности должно предусматриваться для защиты от коррозии конструкций из алюминия.. Участки конструкций, на которых нарушена целостность защитной анодной или лакокрасочной пленки в процессе сварки, клепки и других процессов, выполняемых при монтаже, после предварительной зачистки должны быть защищены лакокрасочными покрытиями с применением протекторной грунтовки.
Для предупреждения коррозии зданий и сооружений применяют разные способы защиты, в том числе металлизацию, окраску лакокрасочными составами, гуммирование и гидрофобизацию.
Металлизацию применяют для защиты металлических и закладных деталей железобетонных конструкций. Используют цинковую или алюминиевую проволоку, толщина слоя наносимого защитного покрытия 0,2...0,5 мм.
Окраску лакокрасочными составами используют для защиты от коррозии металлических конструкций. Применяют масляные краски, лаки, эмали на основе синтетических смол, битумные мастики и растворы. Защитное покрытие состоит из грунтовки и покровных слоев, количество которых зависит от назначения покрытия, свойств защищаемого материала, технологических условий процесса нанесения и эксплуатации покрытия.
Грунтовку наносят на очищенную и сухую поверхность, она не должна иметь на окрашиваемой поверхности пропусков, подтеков и других дефектов, поэтому она наносится тонкими слоями (желательно не менее двух). На подготовленное грунтовкой основание наносят основные слои окраски. Количество слоев определяют в зависимости от назначения покрытия, технологического процесса нанесения, свойств защищаемого материала и условий эксплуатации покрытия Нанесение покрытия несколькими слоями сводит к минимуму проникновение агрессивной среды через возможные поры одного и даже двух слоев. Покрытие одним слоем большой толщины приводит, как правило, к появлению трещин, нарушению сплошности покрытия и плохой прилипаемости (адгезии) к основанию. При многослойном нанесении покрытия каждый последующий слой наносят после полного высыхания и отвердения предыдущего.
Окраску производят механизированным и ручным способами. При механизированном способе используют пневматические или механические распылители. При окраске малых форм, конструкций решетчатой структуры, в труднодоступных местах во избежание больших потерь лакокрасочных материалов более предпочтительна ручная окраска.
Гуммирование — нанесение на поверхность сырой резины с последующей вулканизацией. На очищенную от грязи и пыли и обезвоженную поверхность наносят тонкий слой резинового клея, на который накладывают листовую или рулонную сырую резину и подвергают температурной обработке — вулканизации. В результате образуется сплошное защитное покрытие толщиной, зависящей от толщины сырой резины (2..А мм). Допускается нанесение на поверхность нескольких слоев раствора сырой резины в бензине. Слои наносят через 40...60 мин после высыхания предыдущего, затем покрытие вулканизируют.
Гидрофобизация — покрытие поверхностей железобетонных и каменных конструкций водными растворами кремнийорганических соединений. На поверхности, покрытой составом, образуется защитная водонепроницаемая пленка, препятствующая проникновению воды и коррозии материалов. Нанесение растворов осуществляют кистями, валиками, краскопультами, другими средствами малой механизации. Покрытие служит 3...5 лет, его необходимо периодически обновлять.
Антикоррозионное покрытие выполняют при положительных температурах. При необходимости работ при отрицательных температурах необходим отогрев основания, применение подогретых составов, тепловая защита выполненных покрытий.
При выборе и устройстве антикоррозионных покрытий следует руководствоваться требованиям СНиП 3.04.03-85. Защита строительных конструкций и сооружений от коррозии, СНиП 2.03.11-85. Защита строительных конструкций от коррозии.

Что бы оставить комментарий войдите
Комментарии (0)